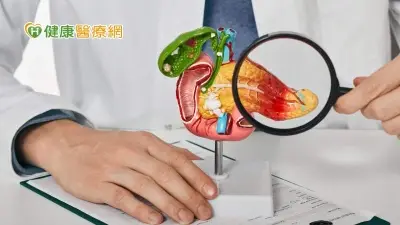
「隱藏版癌王」胰臟癌轉移、惡化速度很快,罹患率與死亡率幾乎一樣,治癒機會低,也是目前預後最差的癌症之一,在台灣癌症死亡率排名第7位。國家衛生研究院與高雄醫學大學研究發現,使用「MEK抑制劑」與「WNT抑制劑」,可有效抑制帶有RNF43基因變異的胰臟癌細胞生長,研究成果登國際期刊。
胰臟位於腹腔深處,腫瘤發生初期幾乎無症狀,發現時通常已是晚期,存活期恐不到半年[i]。現有的治療方法除外科手術外,還有放射線治療、化學藥物治療及免疫治療等,但治療成效仍有限,如何提升病人的存活率是一大挑戰。
胰臟癌四大變異基因
國家衛生研究院癌症研究所特聘研究員洪文俊表示,臨床統計發現大約有6至10%的胰臟癌病人,帶有RNF43基因突變。RNF43是調控蛋白質WNT訊息傳遞路徑的一個穿膜蛋白。
K-RAS
TP53
CDKN2A
SMAD4
洪文俊與高雄醫學大學講座教授陳立宗的合作研究團隊首度證實,B-RAF為一新穎之RNF43泛素化標靶蛋白。帶有RNF43基因變異的胰臟癌細胞,對於MEK抑制劑特別敏感,經過大規模篩選MEK上游的調控蛋白後,可泛素化B-RAF,並加速B-RAF蛋白分解。當RNF43突變失去活性時,B-RAF蛋白會增加進而活化下游的MEK及MAPK,造成細胞過度生長及癌化。
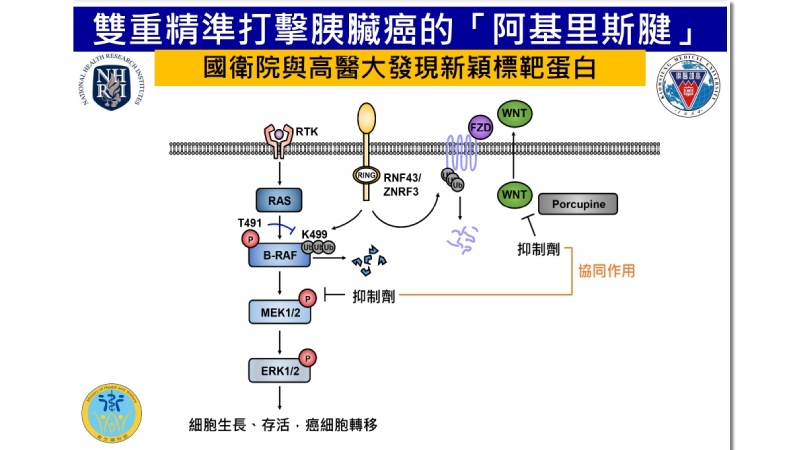 ▲使用「MEK抑制劑」與「WNT抑制劑」,可有效抑制帶有RNF43基因變異的胰臟癌細胞生長。(國衛院提供)
▲使用「MEK抑制劑」與「WNT抑制劑」,可有效抑制帶有RNF43基因變異的胰臟癌細胞生長。(國衛院提供)
雙刀流擊殺變異基因
洪文俊指出,在細胞及小鼠模式實驗中證實,共同使用MEK抑制劑與WNT抑制劑,對帶有RNF43變異的胰臟癌細胞,具強烈的協同毒殺效果,可有效抑制腫瘤的生長,研究成果已於今年1月發表於國際期刊《先進科學》(Advanced Science)。
陳立宗表示,胰臟癌的治療以往以化學治療為主,只有一種BRCA2突變基因有標靶藥物可做為維持性治療,除此之外幾乎沒有精準醫療。健保署規劃於今年5月將癌症病人次世代基因檢測納入健保給付,期望此研究成果能作為未來胰臟癌治療上的參考,對於個人化精準醫療提供更大的助益。
研究論文全文:https://pubmed.ncbi.nlm.nih.gov/38225722/
[i] https://www.cgh.org.tw/ec99/rwd1320/category.asp?category_id=934